お知らせ
先進医療として承認
「自己骨髄由来培養間葉系細胞移植による末梢動脈疾患に対する完全自家血管新生治療法」
~虚血による下肢切断の回避、疼痛軽減を目指して~
2022.06.01
報道関係者各位
ニュースリリース
2022年6月1日
先進医療として承認
「自己骨髄由来培養間葉系細胞移植による末梢動脈疾患に対する完全自家血管新生治療法」
~虚血による下肢切断の回避、疼痛軽減を目指して~
【概要】
このたび、東京医科大学病院(病院長:山本謙吾/東京都新宿区)細胞・再生医療センター長で心臓血管外科の福田尚司教授を中心としたチームにより、自己骨髄由来培養間葉系細胞移植による末梢動脈疾患に対する完全自家血管新生治療法が、先進医療制度の承認を受けました。(2022年4月1 日より算定開始)
これにより、虚血による下肢切断の回避、あるいは著しい疼痛のための苦しみが軽減されることが期待されます。今後、この治療法を通して有効性・安全性を明らかにし、多くの下肢虚血の患者さんに幅広く実施できるように保険収載を目指します。
【本治療法実施のポイント】
- 閉塞性動脈硬化症のうち最重症例である重症下肢虚血の患者さんを対象にします。
- 他の既存治療の実施が不可能か困難な場合に限り、本治療法の対象となります。
- 患者さん自身の血液で、自身の少量骨髄を病院内の細胞調製室で培養します(写真1)。
- 培養された細胞(自家骨髄培養間葉系細胞)が2週間ほどして一定数になったところで(写真2)、入院し下肢筋肉内に投与します(写真3、4)。
- 投与後は定期的に検査を実施します。
- 費用は先進医療の規則により、自費診療部分と保険診療部分に分けられます。
- 本治療法は先進医療として実施されますが、有効性・安全性を検討する研究という形をとっています。

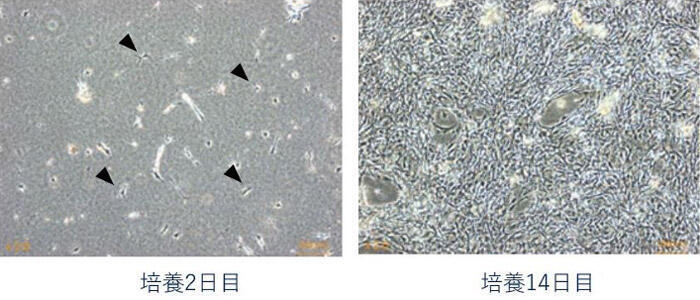
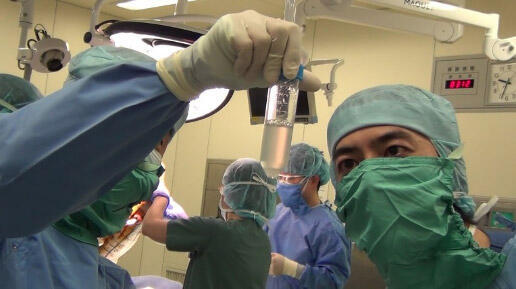
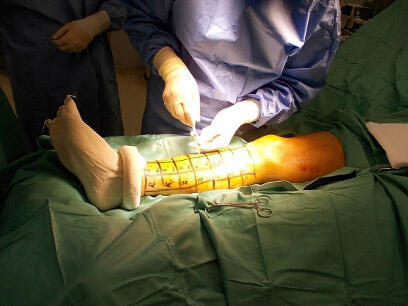
以下に、本治療法実施(研究登録)の流れを示します。

【研究の背景】
閉塞性動脈硬化症は、四肢の末梢動脈に狭窄や閉塞が起こることで血流が低下し、間欠性跛行(歩くと足が痛い症状)、安静時疼痛、下肢の組織障害(皮膚潰瘍・壊死)などの症状を引き起こす疾患です。人口の高齢化や食生活の欧米化による生活習慣病患者の増加等に伴い閉塞性動脈硬化症患者数は増加の一途を辿っていますが、依然として既存の治療法では閉塞性動脈硬化症の重症患者においては死亡率が高く、また、下肢切断を余儀なくされる患者さんは年間30%1)と言う現状があり予後が非常に不良です。
近年、薬物治療や血行再建術に限界のある重症の末梢動脈疾患に対して、自己末梢血または自己骨髄由来の幹細胞を虚血四肢骨格筋へ筋肉内移植することにより、虚血部周辺の組織からの血管新生の増強や側副血行の発達を促すことで、虚血組織の血流を確保し、組織障害や壊死を軽減させようとする試みがなされています2)。
2021年現在、国内で実施されている血管再生医療は、遺伝子治療薬を用いる方法、あるいは、G-CSF(顆粒球コロニー形成刺激因子)を投与し、アフェレーシスを用いる方法がありますが、安全性および侵襲性の点で問題が残されています。
私たちの治療法では、自己骨髄を少量のみ局所麻酔下で採取し、自己血由来の多血小板血漿を用い、病院内の細胞調製室において培養し使用するため、既存療法に比べ、安全性がより高く低侵襲と考えております。
また、2018年末で、わが国の透析患者さんは339,841名3)で、その4.9%、つまり1万6千人以上4)の透析患者さんが重症下肢虚血であると考えられます。既存の再生医療製品では、慢性透析患者さんへの効果が不確定で、適応外とされている場合もあります。
そこで、私たちは、基礎検討5)を経て、2016年から、閉塞性動脈硬化症患者さんにおいて最重症である安静時痛あるいは下肢の組織障害(皮膚潰瘍・壊死)を呈する重症下肢虚血の患者さんのうち、繰り返す血行再建術(カテーテル治療あるいはバイパス術)に対し効果を認めない血行再建抵抗性の患者さん、あるいは、解剖学的理由から血行再建が困難な患者さんに対し、患者さん自身の少量骨髄間葉系細胞を自己血より調製した多血小板血漿を用いて培養し、その細胞を下肢筋肉内に投与する臨床研究(PB3150012)を実施してきました。多血小板血漿とは血液中の血小板を高濃度に濃縮させたもので、血小板には種々の細胞成長因子が含まれており、すでに多血小板血漿を用いる培養法が開発されています6)。 この方法では動物由来の試薬を使わず患者さん自身の細胞を使用するために、安全性が高く免疫学的拒絶反応などを避けることが可能であり、細胞調製室を備えた施設において比較的容易に実施することが可能な治療と考えています。
【本研究で得られた結果・知見】
先行臨床研究の結果は、投与患者数は5名、そのうち4名は重症糖尿病で、3名が慢性腎臓病ステージ5(慢性透析)でした。投与後1年間の経過観察期間を経て、安全性と一定の有効性が示されました。
以下に結果を示します。
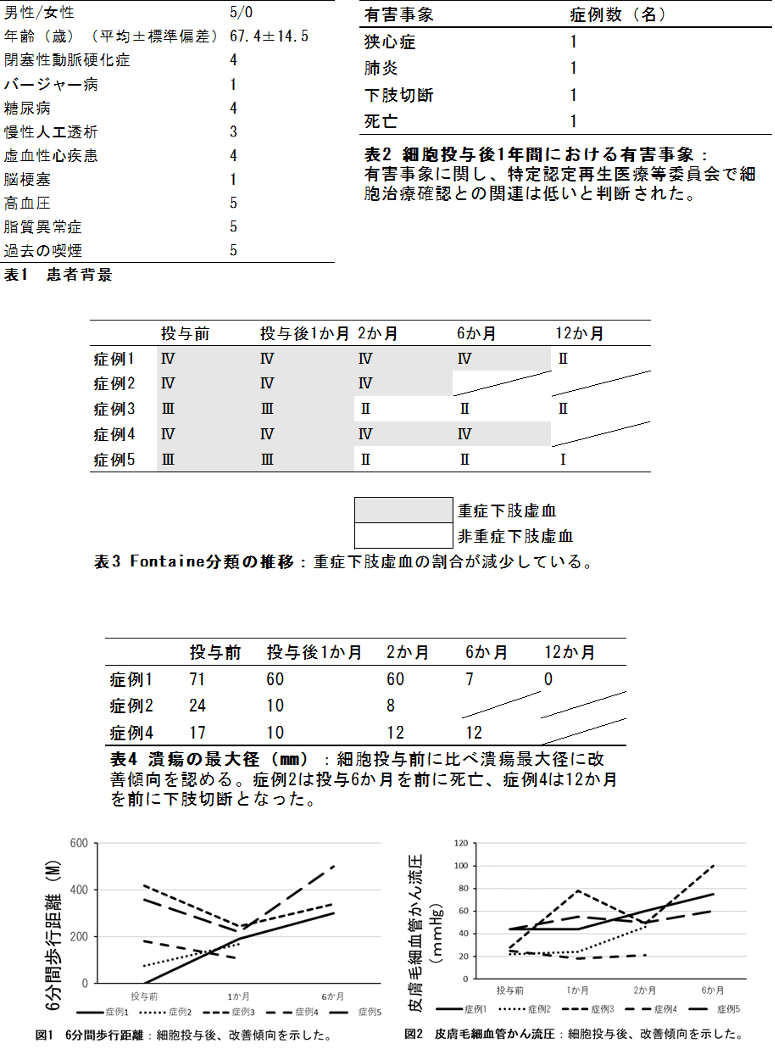
【今後の展開および波及効果】
私たちの骨髄由来培養間葉系細胞移植は、完全自家で培養可能なため、高い安全性を有し、重症糖尿病や透析患者さんを含む重症の末梢動脈疾患に対し安全で有用な治療法になり得ると考えられます。
今回、先行臨床研究の結果をもって先進医療の実施承認を得ることができました。今後、先進医療を通して、より進んだ形で本治療法の有効性・安全性を明らかにし、多くの下肢虚血の患者さんに幅広く実施できるように保険収載を目指します。
【参考文献】
- 1) 日本脈管学会 下肢閉塞性動脈硬化症の診断・治療指針Ⅱ.2015,p19.
- 2) Tateishi-Yuyama E. Matsubara H, Murohara T, et al. Therapeutic angiogenesis for patients with limb ischaemia by autologous transplantation of bone-marrow cells: a pilot study and a randomized controlled trial. Lancet 360: 427-435, 2002.
- 3) わが国の慢性透析療法の現況. 透析会誌52(12):679~754,2019.
- 4) 透析患者のASOの実態調査. 透析会誌43(2):177~182,2010.
- 5) Fukuda S, Hagiwara S, Fukuda S, et al. Safety assessment of bone marrow derived MSC grown in platelet-rich plasma. Regen Ther. 2015 Mar 23;1:72-79.
- 6) Katharina Schallmoser, Christina Bartmann, et al. Human platelet lysate can replace fetal bovine serum for clinical-scale expansion of functional mesenchymal stromal cells. TRANSFUSION 47: 1436-1446, 2007.
【代表研究者コメント(福田尚司 東京医科大学病院 細胞・再生医療センター長)】
本治療法は、2011年に国立国際医療研究センター(東京都新宿区)で基礎検討が始まり、2018年からステージを東京医科大学に移し、この間、多くの諸先生方、多職種の方々のご援助をいただき、2022年1月に先進医療実施の承認をいただくことができました。
こうした多くの方々の「虚血による足の切断を回避したい」という思いを持って、今回の先進医療を実施して参ります。
<先進医療承認までの経緯>
| 2011年 | 国立国際医療研究センターにて、基礎実験を開始 |
|---|---|
| 2015年 | 基礎実験のまとめを発表(Regen Ther. 2015 Mar 23;1:72-79) |
| 2016年 | ヒトに対する前向き介入研究を開始(PB3150012) |
| 2018年 | 同研究を終了 東京医科大学病院に赴任、病院内に細胞調製室を設立 |
| 2019年 | 同細胞調製室が関東信越厚生局にて承認(FC3190200) |
| 2021年 | 本先進医療研究が本学特定認定再生医療等委員会で承認 |
| 2022年 | 同研究が厚生労働省先進医療会議で承認 |
〇先進医療に関する問い合わせ(患者さん向け)
(お問い合わせの際は「血管新生先進医療」とお申し出ください。)
東京医科大学病院
細胞・再生医療センター
TEL:03-3342-6111(病院代表)
Mail:
HP:https://hospinfo.tokyo-med.ac.jp/shinryo/saisei/index.html
〇参加に関する問い合わせ(医療従事者向け)
東京医科大学病院
心臓血管外科 教授 福田尚司
TEL:03-3342-6111(病院代表)
Mail:
〇報道に関する問い合わせ
学校法人東京医科大学
企画部 広報・社会連携推進室
TEL:03-3351-6141(大学代表)
Mail:
