お知らせ
『悪性脳腫瘍に対する光線力学的療法で世界をリード』
~医師主導治験で初発GBM(膠芽腫)の12か月生存率100%を達成~
2013.02.01
報道関係者各位
ニュースリリース
2013年2月1日
悪性脳腫瘍に対する光線力学的療法で世界をリード
~医師主導治験で初発GBM(膠芽腫)の12ヶ月生存率100%を達成~
悪性脳腫瘍の新たな治療法を開発
東京医科大学は悪性脳腫瘍に対する光線力学的療法(PDT)を新たに開発、東京女子医科大学との共同研究グループを通じて医師主導臨床試験(治験)を終了しました。PDTは、腫瘍組織や新生血管への集積性がある光感受性物質を患者に投与します。そして、同物質が集まった箇所の組織にレーザー光を照射し、光感受性物質に光化学反応を引き起こして活性酸素を発生させ、がん細胞を変性・壊死させる治療法です。正常な細胞を傷つけるリスクが少ないというメリットがあり、国内では早期肺がん治療の適応で承認されていますが、PDTが悪性脳腫瘍に適用され治療法として開発されたのは国内では今回が初めてです。
※医師主導臨床試験:医師や医療機関が主導して非営利で行う臨床試験のこと。手術や他の療法等との組み合わせも考えて、
治療法の安全性や有効性を調べる場合など、製薬メーカーや医療機器メーカーなどから治験薬や機器の提供を受けて治験を行い、
そのデータをもとにメーカーが承認申請します。
国内外から注目を集める画期的な治験データ
悪性脳腫瘍のなかで今回治験の対象となった初発GBM治療に関して、世界でこれまで最もよい成績をあげた報告例は、12ヶ月OS率(治療1年後の生存率)が61.6%でした。それに対して、東京医科大学が東京女子医科大学と行なった医師主導臨床試験では、初発GBMの患者13症例について12ヶ月OS率が100%(全員が生存)でした。さらに、これまでの平均生存日数14.6ヶ月に対して、今回の試験では24.8ヶ月を実現しました。今後、これらの治験データをもとに製薬メーカーと医療機器メーカーが悪性脳腫瘍に対する薬剤と装置の適用拡大を目指す薬事承認を年内に申請、来年秋までには認可される見通しです。
※初発GBM:最初にできる腫瘍を「初発」といい、「再発」と区別します。GBMは膠芽腫(中枢神経系腫瘍)のことで、
臨床的に最も悪質な腫瘍といわれています。
本大学の秋元准教授が第33回日本レーザー医学会総会賞を授与
2012年11月10、11日に大阪大学吹田キャンパスにて開催された「第33回日本レーザー医学会総会」において、200題におよぶ演目のなかから臨床系分野で東京医科大学脳神経外科学講座の秋元治朗准教授が総会賞に選ばれました。
※日本レーザー医学会:レーザーに関する医学、生物学及び工学における研究と技術の向上のため、学術大会の開催等により、
医学と医療の発展及び学術交流を図り、社会に貢献することを目的として設立された学会です。
●治療が難しい悪性脳腫瘍
脳腫瘍には良性と悪性がありますが、悪性腫瘍のなかでもGBM(glioblastoma 膠芽腫・こうがしゅ)は最も悪性で治療が難しい腫瘍です。 |
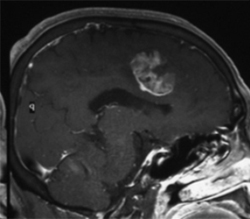 右前頭葉の内側面に発生した膠芽腫 |
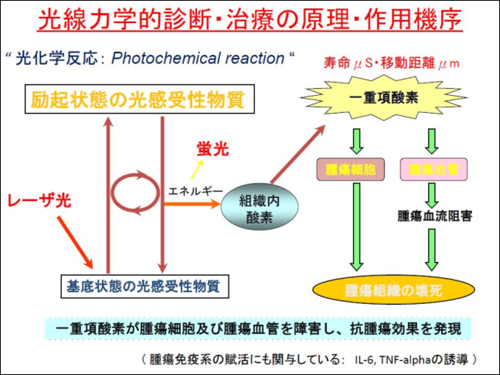
●光線力学的治療の仕組みと特徴
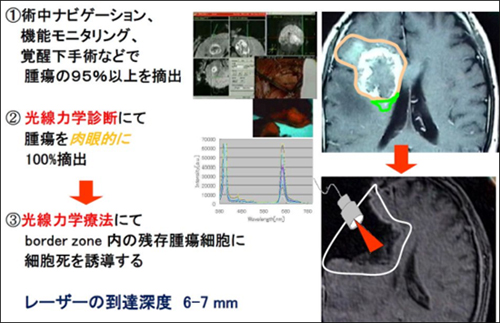
難しいといわれる悪性脳腫瘍に関して、有望な治療法のひとつが光線力学的療法(PDT)です。PDTは、開頭による脳腫瘍切除術と併用して行われます。先ず、手術前の段階で患者に腫瘍組織や新生血管への集積性がある光感受性物質を投与します。そして、脳外科手術にて開頭し腫瘍を切除します。しかし、このGBMは正常な細胞と見分けづらいため、手術では腫瘍を取り残している可能性もあります。そこで、事前に投与した光感受性物質が集まった箇所にレーザー光を照射し、光感受性物質に光化学反応を引き起こして活性酸素を発生させ、手術で取りきれなかったがん細胞を変性・壊死させます。
PDTの大きなメリットは、悪性腫瘍を狙い撃ちにするため正常な細胞を傷つけるリスクが少ないという点です。また、一般的な高出力のレーザー治療とは異なり、手をかざしてもほとんど熱さを感じない程度のレーザー光を用いるため、患者への侵襲性が少ないなどの特徴があります。
 |
 |
●東京医科大学におけるPDT研究開発の取組み
悪性脳腫瘍のPDT治療については、日本をはじめ世界各国で以前から研究開発が行われてきました。しかし、レーザー光は深さ1センチ未満の腫瘍組織にしか届かず進行がんには十分な効果が期待できないことや、人間の脳細胞に対する本レーザー光照射についてそれまで例がないなど、いくつかの課題がありました。
そうしたなかで、東京医科大学は15年ほど前からPDTの研究開発に取り組み、初めて早期肺がん治療の保険承認を受けるなど、国内におけるPDTのパイオニアとして肺がんにおいて大きな成果をあげる一方で、悪性脳腫瘍に関しても基礎実験を繰り返してきました。
そして、2009年からは東京女子医科大学とともに医師主導臨床試験(治験)を開始し、初発GBMの患者13症例について12ヶ月OS率が100%、さらに、これまでの平均生存日数14.6ヶ月を大幅に伸ばす24.8ヶ月を実現するなど、治験効果を証明することができました。現在は、これらの治験データをもとに製薬メーカーと医療機器メーカーが悪性脳腫瘍に対する薬剤と装置の適用拡大を目指す薬事承認を2012年12月に申請、本年秋までには日本発の悪性脳腫瘍に対するPDT治療が世界で初めて認可される見通しです。
●PDTは「第一世代」からオールジャパン発の「第二世代」へ
今回の医師主導臨床試験では、光感受性物質としてMeiji Seikaファルマの腫瘍親和性光感受性薬剤「レザフィリン(一般名 タラポルフィンナトリウム)」を投与し、パナソニックヘルスケア製の半導体レーザー装置「PDレーザ」を脳に照射しました。これらはいずれも日本で開発されたもので、これまでの薬剤およびレーザー装置に対して、いわば第二世代とも呼べる進化を遂げています。 |
 光線力学的治療薬剤:レザフィリン® |
 半導体レーザー装置:PDレーザ® |
●今後の課題
医師主導臨床試験のレーザー照射は、低出力のものを1-2回のみという条件で行われたにも関わらず、世界をリードする治療成果をあげることができました。
今後はレーザーのパワーアップや反復照射、そして薬剤の効き目を強くするというように治療条件を変え試験データを積み重ねていきながら、東京医科大学では悪性脳腫瘍へのPDTについて治療効果をさらに高めていきたいと考えています
東京医科大学病院
企画広報室
■東京医科大学 脳神経外科ページ
http://team.tokyo-med.ac.jp/nou/
〒160-0023 東京都新宿区西新宿6-7-1
TEL:03-3342-6111(代)
URL:http://hospinfo.tokyo-med.ac.jp/
